Strengthening
Regulatory Systems
The ARN: Le réseau africain de réglementation pharmaceutique





Le réseau africain de
réglementation pharmaceutique (ARN)
Le réseau africain de réglementation pharmaceutique - en anglais African Regulatory Network (ARN) - est un réseau ad-hoc créé par notre organisation. En partenariat avec les autorités de réglementation, l'industrie pharmaceutique, ainsi qu'avec les autres parties prenantes de la réglementation, l’ARN vise à encourager l'harmonisation et la convergence des exigences en matière de réglementation pharmaceutique en Afrique. L'ARN cherche à favoriser un accès rapide et large à des produits médicaux innovants et de qualité, pour le bénéfice des patients.

![]()
NOTRE ACTION
Renforcer les capacités en Afrique
![]()
NOTRE OBJECTIF
Des systèmes de réglementation en phase
![]()
NOTRE STRATEGIE
Concept des 6 "C"
Nous estimons que la population en Afrique doit pouvoir accéder à des médicaments et à des vaccins de qualité, dont l’efficacité et l’innocuité sont prouvées. Des systèmes de réglementation pharmaceutique cohérents et fiables s’avèrent indispensables pour atteindre cet objectif. De tels systèmes reposent sur des standards, des normes, des directives, des spécifications et des procédures, définis de façon à garantir la disponibilité de médicaments et de vaccins sûrs. A contrario, des systèmes de réglementation pharmaceutique inefficaces, voire leur absence, peuvent être la cause d’une qualité de médicaments médiocre, de contrefaçons, de négligence d’informatisation des effets secondaires, et constituer un frein à la mise à disposition de traitements indispensables aux patients.
Le réseau africain de
réglementation pharmaceutique (ARN)

1er pilier : Notre action : renforcer les capacités en Afrique
Contribuer à la connaissance scientifique dans le domaine de la réglementation
- Illustrer, à l’attention des acteurs de la réglementation pharmaceutique en Afrique comment développer des processus réglementaires solidement basés sur la science, ainsi que sur les progrès technologiques et l’innovation;
- Favoriser davantage l’harmonisation et la convergence des systèmes de réglementation; et
- Assister techniquement les pays afin qu’ils puissent faire face aux priorités réglementaires.
Aider à combler les lacunes
- Soutenir la réglementation pharmaceutique nationale et régionale dans :
- la définition de normes et de standards
- le renforcement des capacités, le développement et l’évaluation des différents processus réglementaires (par ex. la préqualification)
- l’évaluation des produits pharmaceutiques en développement (par ex.: au niveau des essais cliniques, de la fabrication ou du contrôle)
- la surveillance post-commercialisation (par ex.: la pharmacovigilance, le suivi des aspects qualitatifs, ou encore la question de la diminution/altération de l’efficacité)
- le développement de plateformes de rencontre et d’échange d’information;
- Faciliter le partage de connaissances afin que l’ensemble des parties prenantes contribuent au développement continu des différents axes ci-dessus, en apportant leurs compétences, forces et expertise propres; et
- Engager un dialogue constructif au sujet de la réglementation pharmaceutique et promouvoir une prise en compte accrue de ces questions dans le cadre de l’élaboration des politiques de santé en Afrique.
Sans une consolidation effective des points faibles de la réglementation pharmaceutique, les nombreuses initiatives entreprises dans le domaine biomédical en Afrique ne pourront pas livrer leur plein potentiel dans les années à venir.
Insuffler un changement en matière de réglementation pharmaceutique
- Remettre en cause les anciens paradigmes et encourager l’innovation en matière de développement et de réglementation des produits médicaux. Ceci englobe la définition d’approches nouvelles et pertinentes de la réglementation afin d’évaluer au mieux le rapport risque/bénéfice des avancées scientifiques, de suivre leur évolution, de les prioriser et d’en mesurer l’impact; et
- Démontrer comment l’expertise et les forces spécifiques à chaque acteur de la réglementation peuvent concourir à l’harmonisation et à la convergence, mener à une meilleure coordination et communication, et contribuer à répondre de façon complémentaire et pragmatique aux déficits de capacité.
Agir avec pragmatisme et de façon adaptée à la réalité africaine
- Améliorer la compréhension des problématiques propres aux différents acteurs, telles que les questions de santé publique, éthiques, commerciales, ou de priorités politiques; et
Prendre en compte ces particularités pour forger des approches pragmatiques à même d’apporter des solutions aux problèmes majeurs de la réglementation, dans l’intérêt des patients.
Le réseau africain de
réglementation pharmaceutique (ARN)
2ème pilier: Notre objectif : des systèmes de réglementation en phase
La compatibilité des systèmes de réglementation pharmaceutique entre eux est essentielle. Pourquoi? Simplement parce que :
- Dans un monde de plus en plus globalisé, aucun acteur ne peut répondre seul aux défis de la réglementation pharmaceutique. L’Afrique ne fait pas exception à cette réalité mondiale.
- Les opportunités de tendre vers plus de convergence existent. Et la nécessité de s’atteler de concert à résoudre des problématiques communes de santé publique fait désormais l’objet d’un engagement qui s’est affirmé et renforcé.
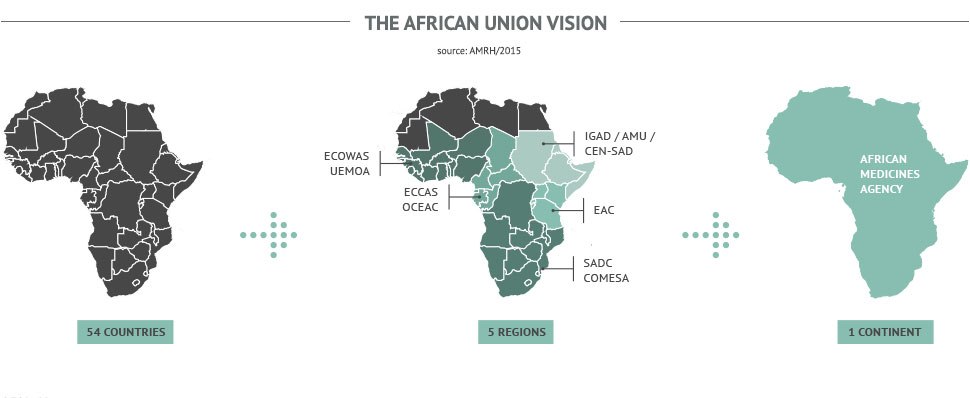
L’ARN vise à :
- Placer la résolution de l’Assemblée mondiale de la santé relative au renforcement des systèmes de réglementation des produits médicaux (WHA 67.20) au centre des actions en faveur de l’amélioration des systèmes de réglementation, et comme moteur principal du changement en Afrique;
- Inscrire l’industrie pharmaceutique, par le biais de l’ARN, dans un rôle d’acteur-clé du renforcement des systèmes de réglementation;
- Tirer les leçons des efforts d’harmonisation entrepris dans le monde et mettre en valeur les exemples de réussites, particulièrement en Afrique, afin de générer et enrichir de nouvelles initiatives potentielles;
- Contribuer à démontrer qu’un engagement en faveur de l’excellence réglementaire est essentiel pour combler les lacunes en matière d’expertise;
- Faire prendre conscience que les difficultés auxquelles est confrontée l’industrie pharmaceutique en lien avec la réglementation lors du processus d’homologation, de fabrication ou dans le cadre de la gestion du cycle de vie des produits, ont des répercussions négatives sur l’approvisionnement en médicaments et vaccins de qualité; et
- Montrer que les initiatives et les approches novatrices au niveau mondial tendent toutes à promouvoir la convergence internationale des normes, à réduire les disparités en matière d’homologation, à évaluer et valoriser de nouvelles technologies, à améliorer la couverture des besoins médicaux, ainsi qu’à renforcer la transparence, de paire avec une protection adéquate des données personnelles.
Le réseau africain de
réglementation pharmaceutique (ARN)
3ème pilier: Notre stratégie : le concept des 6 “C”
Construit autour de six principes-clés, notre stratégie repose sur la riche expérience développée par l’Asie en matière de convergence réglementaire. Garantie d’une approche rationnelle et efficace, ce concept des 6 “C” consiste à placer la coopération, la collégialité, la compétence, l’engagement, la communication et la convergence – en anglais Cooperation, Collegiality, Capacity, Commitment, Communication and Convergence – au centre des actions visant à faire converger ou à harmoniser les systèmes de réglementation pharmaceutique. Sa pertinence s’étend à toutes les régions du monde où s’engagent des démarches similaires.
Nous en appelons donc à développer l’agenda de la réglementation pharmaceutique en Afrique sur la base de ce concept. En voici les raisons :
La coopération
- permet de répondre aux contraintes de ressources des agences chargées de la réglementation, et
- évite une duplication des tâches qui en compromettrait l’efficacité, tout en facilitant le partage de savoir-faire.
La collégialité
- facilite l’identification d’objectifs communs et de solutions partagées afin de répondre conjointement aux besoins de santé publique, et
- crée des espaces propices à établir des relations de confiance.
La compétence
- répond au besoin de renforcer le savoir-faire dans le domaine de la réglementation pharmaceutique, notamment par le développement :
- des compétences techniques et de gestion, et
- de plateformes à vocation de rencontre, d’apprentissage et d’échange d’information, et
- favorise l’émergence de solutions novatrices et pragmatiques en matière de réglementation pharmaceutique.
L'engagement
- assure une allocation appropriée de ressources aux différentes fonctions de réglementation pharmaceutique, et
- apporte le soutien nécessaire à une mobilisation proactive et une implication sérieuse dans le cadre d’initiatives de collaboration.
La communication
- accroît la transparence et la prévisibilité tout au long du processus de réglementation, et
- facilite les échanges d’information.
La convergence
- facilite la cohérence des exigences de la réglementation,
- réduit les problématiques nationales spécifiques, et
- rend possible une acceptation et une surveillance globales des produits médicaux.